Die AG Esser analysiert die Rolle das Arylhydrocarbonrezeptors (AHR) für die Immuntoxikologie, hier insbesondere für Haut und Darm. Der AHR ist ein Transkriptionsfaktor, der erst nach Bindung von niedermolekularen Substanzen aktiv wird. Solche Substanzen können aus Nahrungspflanzen stammen, von Darmbakterien aus der Aminosäure Tryptophan erzeugt werden, oder sogar in der Haut durch UV-Strahlung aus Tryptophan entstehen. Umweltschadstoffe wie Dioxine sind auch in der Lage, den AHR zu aktivieren. Der AHR ist wichtig für den Fremdstoffmetabolismus des Körpers einerseits, andererseits auch für die Entwicklung und zahlreiche Funktionen des Immunsystem, wie die Ausschüttung entzündlicher Zytokine. Ziel unserer Arbeit ist die Grundlagenforschung, die zur Nutzung des therapeutischen Potentials von AHR-Liganden führen kann. Die AG Esser hat im Tiermodell der Maus gezeigt, dass der AHR eine wichtige Rolle für eine gesunde Hautbarriere oder für die orale Toleranz spielt, an der Funktion von Hautimmunzellen beteiligt ist, und im Darm die Darmflora mit beeinflussen kann. Wir untersuchen daher die Rolle des AHR für typische Hautimmunzellen, die Darmflora nach z. B. Belastung mit Dioxinen oder „westlicher“ Ernährung. Weitere Projekt zielen darauf ab, in humanen Hautmodellen Immunzellen zu integrieren, um deren Rolle in der Hautkrebsbekämpfung zu untersuchen. Die AG hat weiterhin ein neues Computertool entwickelt, mit dem sich einfach Veränderungen in der Zusammensetzung von Bakterien in Darm oder Haut aus Durchflußzytometriedaten analysieren lassen (FlowSoFine™).

Arbeitsgruppenleiterin:
Charlotte Esser
Rolle des AHR und von Dioxinen für Veränderungen des Darmmikrobioms
Unerwünschte Wirkungen auf das Immunsystem und den Stoffwechsel sind Kennzeichen der schädlichen Wirkungen von Dioxinen und anderen sogenannten persistierenden organischen Umweltschadstoffen (POPs). Diese Schadstoffe sind nach wie vor in der Umwelt vorhanden. Die Wirkungen von gerade geringer Aufnahme von Dioxin auf den Darm und das Darmimmunsystem oder die Darmflora sind wenig untersucht, obwohl die orale Aufnahme den Hauptweg darstellt. Umgekehrt hat die jüngere Forschung gezeigt hat, dass pflanzliche Nahrungsmittelinhaltsstoffe den AHR-Signalweg im Darm günstig beeinflussen, anti-entzündlich wirken und die Darmbarriere schützen. Die Zusammensetzung der Darmflora spielt dabei eine wichtige Rolle. Es ist fast völlig unbekannt, wie Dioxine und andere persistierende organische AHR-Liganden das Darmmikrobiom schädigen und damit negative Veränderungen des Immunsystems oder Stoffwechsels bewirken könnten. Wir fanden in Mäusen derartige Veränderungen im Bakterienprofil bei einer sehr niedrigen Gabe von Dioxin (2,3,7,8-TCDD) über einen längeren Zeitraum. Beachtenswert waren dabei Unterschiede zwischen den beiden Geschlechtern. Dies gilt es weiter zu erforschen. Wir entwickelten ein bioinformatisch unterstütztes Messverfahren (FlowSoFine™) zum einfachen Bestimmen der Zusammensetzung von Mikroorganismen im Darm oder auf der Haut, das wir für diese und viele andere Fragestellungen nutzen können. Das Projekt wurde durch die Deutsche Forschungsgemeinschaft (DFG) gefördert (ES103/9-1).
Die Darm-Haut Achse - Bakterien, AHR-Liganden und atopische Dermatitis
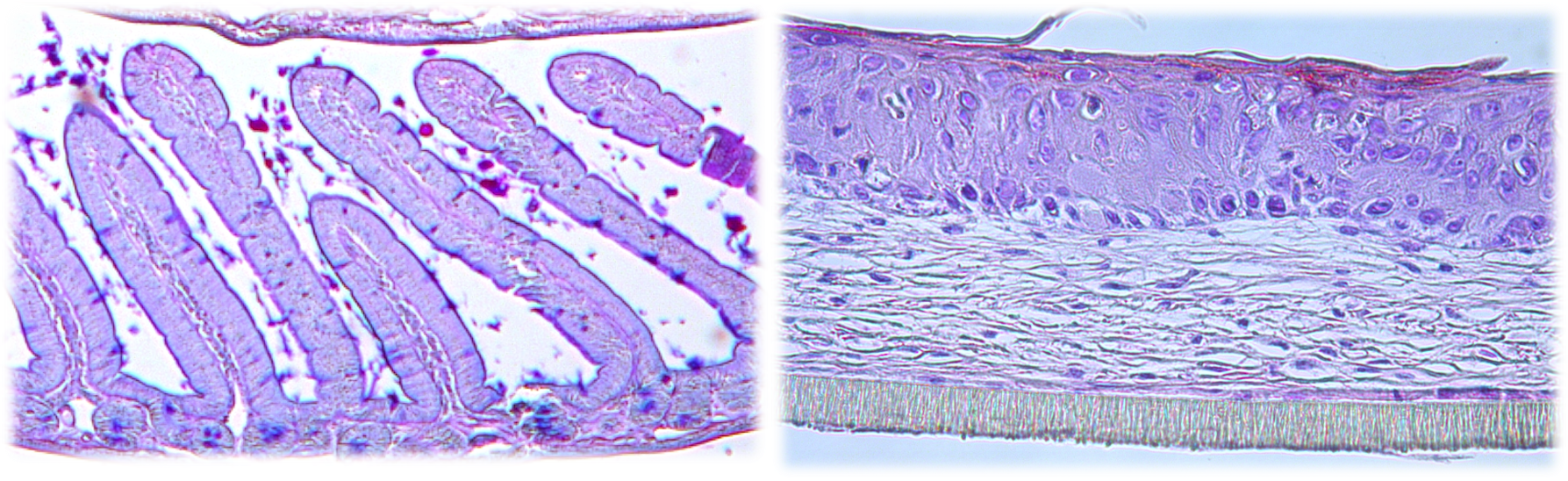
Die Haut und besonders die Epidermis stehen als äußerste Barriere im ständigen Wechselspiel mit der Außenwelt und sind aktiv in die Immunantwort eingebunden. Störungen der Barrierefunktion der Haut können ernste gesundheitliche Folgen haben. Die Haut ist immer von vielen Mikroorganismen besiedelt und es gibt zunehmend Hinweise für deren – positive – gesundheitliche Bedeutung. So sind Schuppenflechte oder atopische Dermatitis Krankheiten, die mit Störungen der Hautbarriere und einer geänderten Zusammensetzung der hautbesiedelnden Bakterien einhergehen. Forschung des IUF hat gezeigt, dass der AHR in allen Zellarten der Haut stark ausgeprägt wird. Wir konnten zeigen, dass ein Fehlen des AHR für die Hautbarriere und die antibakterielle Kontrolle durch Immunzellen der Haut relevant sein kann und dass umgekehrt auch die Aufnahme von AHR-Liganden aus der Nahrung für die Hautbarriere nötig sind. Wir analysieren, wie und ob das Darmmikrobiom, das AHR-Liganden generieren kann, und damit eine ausreichende AHR-Ligandenversorgung aus dem Darm erzeugt, mit einer guten Hautbarriere zusammenhängen und eventuell zu einer Verbesserung einer Hautentzündung beitragen kann (Modell der atopischen Dermatitis). Das Projekt ist darüber hinaus eng mit unserem Projekt verknüpft, in dem wir uns mit den epidermalen γδ-T-Zellen beschäftigen, die für eine stabile Hautbarriere und Immunabwehr relevant sind. Dies ist ein Projekt der Forschungsgruppe 5489 der Deutschen Forschungsgemeinschaft (DFG) (ES103/11-1).
Epidermale γδ-T-Zellen der Maus – AHR als „Entzündungsbremse“
Die Haut enthält nicht nur die bekannten „normalen“ T-Zellen wie sie im gesamten Körper zu finden sind, sondern zusätzlich eine bestimmte Subpopulation von T-Zellen. Diese sogenannten γδ-T-Zellen sind für die Aufrechterhaltung der Gesundheit der Haut, für Wundheilung und gegen Tumorentstehung in der Haut sehr wichtig. Wir fanden, dass diese γδ-T-Zellen in AHR-defizienten Mäusen nach der Geburt fast vollständig verschwinden, obwohl sie normal im fötalen Thymus gebildet werden. Darüber haben wir sehr gute Hinweise, dass die Ausprägung des AHR in diesen Zellen nötig ist, um überschießender entzündliche Aktivität einzuhegen. Mit anderen Worten, der AHR funktioniert als eine Art Entzündungs-Bremse. Hiermit haben wir ein neues Prinzip für die Funktion des AHR in diesen Zellen entdeckt. Unsere weitere Arbeit zielt darauf ab, wie der AHR dies bewirkt, z. B. durch Beeinflussung des Energiehaushaltes oder Regulation von Aktivierungsproteinen. Dieses Projekt wird von der Deutschen Forschungsgemeinschaft (DFG) gefördert (ES103/10-1).
Epidermale γδ-T-Zellen beim Menschen – Rolle in der Krebsbekämpfung
Die Rolle der γδ-T-Zellen in der Bekämpfung des weißen Hautkrebses in humaner Haut wollen wir in einem weiteren Projekt erforschen. Der weiße Hautkrebs, generell auch als ´Non-Melanoma Skin Cancer´ bekannt, ist der häufigste Tumor weltweit, mit stetig steigender Tendenz. Wichtig, aber bisher ganz unzureichend erforscht, sind in der Haut lokal vorhandene Zellen des Immunsystems, die entartete Zellen erkennen und abtöten können. Wir wollen daher erstmals ein γδ-T-Zell-kompetentes 3D-Hautmodell aufbauen. Das Modell soll dann dazu verwendet werden, um die Potenz von γδ-T-Zellen im Erkennen und Eliminieren von Tumorzellen im Gewebeverband der Haut zu analysieren und die Frage zu beantworten, welche Rolle der Arylhydrocarbonrezeptor, der als Sensor für UV-Lichtstress in der Haut gilt, hierbei hat. Dieses Projekt wird von der Wilhelm Sander-Stiftung gefördert (www.sanst.de).
IUF-intern:
AG Haarmann-Stemmann
AG Krutmann
AG Schins
AG Ventura
AG Weighardt
National:
Irmgard Förster, Universität Bonn
Karin Loser, Universität Oldenburg
Christiane Opitz, Deutsches Krebsforschungszentrum, Heidelberg
Astrid Westendorf, Universität Duisburg-Essen
Thomas Tüting, Universität Magdeburg
Stefan Janssen, Universität Giessen
Katja Ickstadt, TU Dortmund
Hyung-Dong Chang, Deutsches Rheumaforschungszentrum, Berlin
Katja Merches, LGL Bayern
International:
Aleksandra Popov, IBRSS, Belgrad, Serbien
Myung-Shin Jeon, INCHEON University, Süd-Korea
Anna Wajda, National Institute of Geriatrics, Rheumatology and Rehabilitation, Warschau, Polen
Die AG Esser betreut die zentrale FACS- und Cell Sorting-Unit des IUF.
Postdocs
Promovierende
Technische Assistenz



